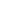捷报频传!凭借精湛的技术实力和卓越的团队协作,2024年2月,博志研新及其子公司再创佳绩,成功推动多个重要产品取得突破性进展,为合作伙伴带来了显著的成果与实实在在的价值!
01-磷酸特地唑胺原料药
2月1日,博志研新的合成技术子公司——新礼泰药业,协助长期合作伙伴研发的磷酸特地唑胺的获得CDE受理(原料药单独审评),并在原料药登记平台公示。
磷酸特地唑胺是一种新型的噁唑烷酮前药抗生素,在体内被磷酸酶快速转化成微生物活性成分特地唑胺。特地唑胺通过与细菌核糖体50S亚基结合抑制蛋白质合成而发挥抗菌作用。特地唑胺抑制细菌蛋白质合成的作用机制与其它非噁唑烷酮类抗菌药物的作用机制不同,因此特地唑胺不大可能与其他类别的抗菌药物发生交叉耐药。
磷酸特地唑胺适用于治疗由下列革兰氏阳性菌的敏感分离株引起的急性细菌性皮肤及皮肤软组织感染(ABSSSI):金黄色葡萄球菌(包括甲氧西林耐药金黄色葡萄球菌[MRSA]和甲氧西林敏感金黄色葡萄球菌[MSSA]的分离株)、化脓性链球菌、无乳链球菌、咽峡炎链球菌群(包括咽峡炎链球菌、中间链球菌和星座链球菌)和粪肠球菌。
在本项目中,新礼泰药业凭借扎实的研发实力,高效完成了磷酸特地唑胺的药学研究及申报资料撰写工作,并得到了合作伙伴的信任和好评。
02-舒更葡糖钠注射液
2月6日,博志研新长期合作伙伴申报的舒更葡糖钠注射液,已获批准上市。
舒更葡糖钠注射液是由荷兰欧加农公司(Organon)研制开发的一种神经肌肉阻滞药物的逆转剂。临床治疗领域为:在成人中拮抗罗库溴铵或维库溴铵诱导的神经肌肉阻滞。对于儿童和青少年(2~17岁)来说,仅推荐本品用于常规拮抗罗库溴铵诱导的阻滞。
2007年,欧加农公司被先灵葆雅(Schering-Plough)收购,到了2009年,先灵葆雅公司与默沙东公司合并,舒更葡糖钠注射液现在由默沙东公司持有并销售。2008年7月25日,舒更葡糖钠注射液获得EMA批准在欧盟上市,2010年1月20日获得PMDA批准在日本上市,2015年12月15日获得FDA批准上市,2017年5月4日获得我国NMPA批准进口上市,上市的规格均是2种规格,分别为2ml:200mg和5ml:500mg,商品名均为BRIDION ®(布瑞亭®),目前均处于上市销售中。
博志研新凭借扎实的研发生产实力,高效完成了舒更葡糖钠注射液的药学研究工作,大大缩短了研发周期,得到了合作伙伴的信任和好评。
03-恩格列净原料药
2月7日,博志研新的合成技术子公司——新礼泰药业,协助合作伙伴研发的化学原料药恩格列净获CDE受理,并在原料药登记平台公示。
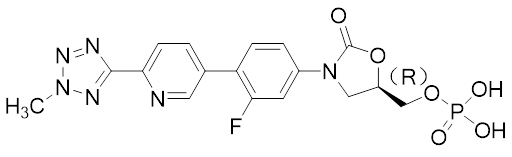
恩格列净(Empagliflozin)是一种具有可逆性、高效性、选择性和竞争性的SGLT-2抑制剂。由美国礼来公司和德国勃林格殷格翰制药公司合作研发。SGLT-2抑制药是一种新型降糖药,主要通过抑制表达于肾脏的SGLT-2,减少肾脏的葡萄糖重吸收,增加尿液中葡萄糖的排泄,从而降低血浆葡萄糖水平。且降糖效果不依赖于β细胞功能和胰岛素抵抗。
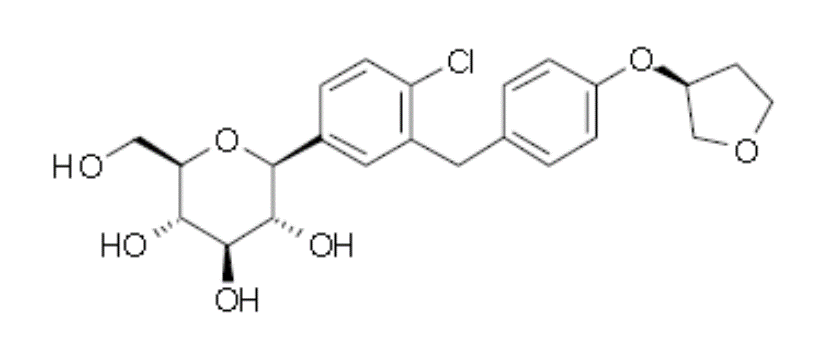
欧盟委员会于2014年5月3日首次批准上市,2014年8月1日获得美国食品药品管理局(FDA)的批准,是FDA继2013年3月29日批准强生制药公司的卡格列净和2014年1月8日批准阿斯利康公司的达格列净之后,第3个具有抑制SGLT-2新作用机制的治疗糖尿病新药。
恩格列净原料药由博志研新合成技术子公司新礼泰药业负责全过程技术服务。新礼泰药业是小分子创新药CMC一体化服务平台,在CMC服务方面有独特优势。在有限的时间内,我公司高效完成了合作伙伴委托的恩格列净研究工作,包括药学研究及申报资料撰写,凭借扎实的研发实力得到了合作伙伴的信任和好评。
04-布立西坦注射液
2月20日,博志研新协助长期合作伙伴申报的布立西坦注射液临床试验申请,国家局已受理。
癫痫是一种由多种病因引起的慢性脑部疾病,以脑神经元过度放电导致反复性、发作性和短暂性的中枢神经系统功能失常为特征。据世界卫生组织(WHO)估计,全球大约有五千万癫痫患者。近年来,我国活动性癫痫患病率为4.6%,年发病率在30/10万左右。据此估算,我国约有600万左右的活动性病患者,同时每年有40万左右新发癫痫患者。抗癫痫药物(antiepileptic drugs,AEDs)治疗是目前癫痫治疗中最常用、最重要的手段,常作为首选方案。
布立西坦是比利时优时比(UCB)公司开发的第三代抗癫痫药,是自2013年以来FDA批准的首个治疗部分性癫痫发作的抗癫痫药物。在中国,2022年抗癫痫药在公立医院和实体药店双终端销售额达到70亿元。布立西坦是左乙拉西坦的结构衍生物,作为第3代新型抗癫痫药具有更好的药动学特征以及中枢神经系统耐受性、安全性,具有良好的用药前景。国内尚无布立西坦注射液获批进口,也没有布立西坦注射液仿制制剂获准上市。因此该项目的研发,将为国内癫痫领域用药提供新选择,使患者受益。
05-JP001片
2月21日,博志研新协助长期合作伙伴申报的改良新药JP001片临床试验申请已获得国家局受理。
JP001片属于2.3、2.4类新药,为复方制剂,拟适应症为联合替莫唑胺合并放疗治疗新诊断的神经胶质母细胞瘤。其活性成分具有药理互补性,其通过自噬双重调节机制使肿瘤细胞对化疗更为敏感,同时可将肿瘤相关巨噬细胞从免疫抑制的M2型转变为M1型,改变肿瘤微环境。
胶质母细胞瘤是星形细胞肿瘤中恶性程度最高的胶质瘤。肿瘤位于皮质下,多数生长于幕上大脑半球各处。呈浸润性生长,常侵犯几个脑叶,并侵犯深部结构,还可经胼胝体波及对侧大脑半球。发生部位以额叶最多见。胶质母细胞瘤生长速度快,70%~80%患者病程在3~6个月,病程超过1年者仅10%。目前的标准治疗为最大化的安全切除,然后对切除腔进行同步放射治疗(RT)和替莫唑胺(TMZ)化疗,随后继续TMZ辅助治疗。
在该项目中,博志研新凭借扎实的研发实力、完善的研发体系,高效的完成了JP001片的药学研究和注册资料的撰写,顺利获得临床试验申请的受理,并得到了合作伙伴的信任与好评。
这一系列成果,不仅证明了博志研新在研发领域的深厚底蕴和卓越能力,更为公司未来的发展铸就了坚实基石。未来,博志研新将满怀信心,以更加昂扬的斗志和更加务实的作风,迎接每一个挑战,共创更加辉煌的未来!